-

- ▲ 카이스트 정문.ⓒ카이스트
국내의 한 연구진이 암 치료법의 새로운 가능성을 제시해 주목을 받고 있다.
18일 한국과학기술원(KAIST)에 따르면 생명과학과 전상용 교수·이용현 박사 연구팀이 ‘빌리루빈’을 항암약물 전달체로 이용하는 기술을 개발했다.
주로 간에서 배설되는 빌리루빈은 적혈구와 세포 안 다양한 효소에 있는 ‘헴’의 최종대사물질이다.
신생아는 간 기능이 성숙하지 못할 때, 성인은 질병이나 피로 등으로 간 기능이 떨어졌을 때 빌리루빈을 배설하지 못한다. 노란색을 띠는 빌리루빈이 몸에 그대로 축적되면 황달을 일으킨다.
황달 치료에는 ‘광선 요법’이 쓰인다. 항산화 작용 특성이 강한 빌리루빈에 빛을 쏘면 산화하면서 친수성(親水性)이 큰 ‘빌리버딘’이라는 물질로 전환되거나 작은 빌리루빈 물질로 깨진다.
-
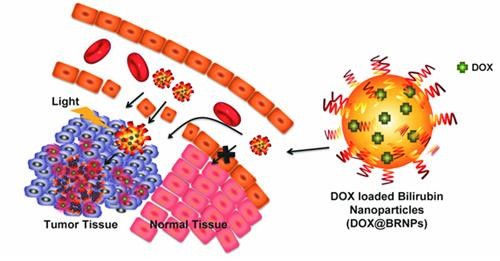
- ▲ 인간 폐암 동물 모델에서 약물이 선적된 빌리루빈 나노입자가 실제 작용하는 모식도.ⓒ카이스트
연구팀은 이 같은 빌리루빈의 특성을 암 치료 물질 전달 시스템에 적용했다.
친수성을 갖는 물질과 빌리루빈을 결합해 나노입자로 만든 후에 항암제인 ‘독소루비신(Doxorubicin)’을 실어 나르도록 했다.
암 부위에 빛을 드러내면 빌리루빈이 와해하면서 선적된 항암제가 암 조직을 공격하는 원리라고 연구팀은 설명했다.
연구팀은 이 시스템이 인간 폐암 동물 모델에서 기존 항암치료 그룹보다 우수한 치료 효능을 보이는 것을 규명했다.
또 연구팀은 암 부위 어느 한 곳에 빛을 쐈을 때 효능이 향상될 뿐만 아니라 운반체인 빌리루빈 나노입자 자체도 일정량의 항암효과를 나타냄을 확인했다.
-
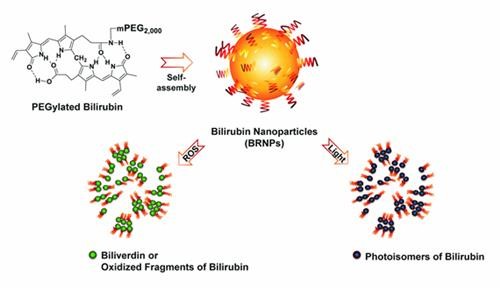
- ▲ 빌리루빈 나노입자가 빛과 활성산소에 의해 와해됨을 보여주는 결과도.ⓒ카이스트
이번 성과는 빌리루빈을 활용한 항암치료용 다중자극감응형 약물전달시스템을 최초로 개발해 원천기술을 확보했다는 의의를 가진다.
공정이 복잡하고 잠재적 독성을 유발할 가능성이 있는 인공소재 기반 자극 감응성 약물 전달체를 대체할 수 있는 가능성을 열었다는 뜻이다.
연구팀은 앞서 지난 5월 ‘빌리루빈이 적절하게 조절된다면 심혈관 질환이나 암 발병 가능성이 작아져 난치성 염증을 치료할 수 있다’는 내용의 연구 결과를 발표하기도 했다.
이용현 박사는 “앞으로 임상 연구를 거치고 적용 가능성을 평가해 궁극적으로 암을 치료하는 새 방안으로 개발되길 기대한다”고 전했다.
한편 이 연구는 한국연구재단 글로벌연구실사업 지원을 받아 수행한 것이다.
전상용 교수·이용현 박사 연구팀…항암약물 ‘기술 개발’
카이스트, 황달 유발물질 이용 ‘암 치료’ 길 열어
- 김동식 기자
입력 2016-08-18 14:00수정 2016-08-22 05:02
공유하기
기사 공유하기
김동식 기자







